Panamá-Chiriquí, viernes 7 y 14 de diciembre de 2012.
http://www.elinformedavid.com/
Por: Dr. Danilo Antonio Castillo G.
 |
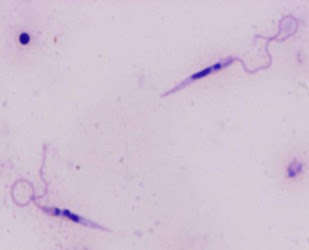
| Flebótomo transmisor de la leishmaniasis |
La leishmaniasis
cutánea y mucocutanea se le conoce también con las siguientes denominaciones:
Botón de Aleppo, de Bagdad o de Delhi; furúnculo oriental; en América:
espundia, uta y úlcera del chiclero. La
leishmaniasis visceral es conocida como Kala-azar.
La primera descripción
de la leishmaniasis tegumentaria fue hecha por El Razi de Irak, en 1500 d.C.
En 1898, Barowsky descubrió el agente etiológico. Leishman en 1903, describió a los parásitos
causantes del Kala-azar. Ese mismo año
Wright redescribió el agente etiológico, llamándole Leishmania tropica. En 1904 Rogers cultivo el agente etiológico
del kala-azar en sangre humana descubriendo la forma de promastigote. Esta especie fue bautizada como L. donovani. Cuatro años más tarde Nicolle y Sicre, lograron
cultivar el agente etiológico del botón de oriente. En 1921 Sergent, Parrot y colaboradores
demostraron que un díptero del género Phlebotomus era el transmisor de la leishmaniasis
tegumentaria. En América la
leishmaniasis era conocida desde la era prehispánica, como lo hacen constar
obras arqueológicas y piezas de cerámicas de forma humana que muestran
mutilaciones de orejas, nariz y boca, así como los cronistas y los religiosos,
que relataron en sus escritos las observaciones de “llagas rebeldes” que
aquejaban los indígenas de ciertas regiones causadas por picadura de mosquito. En la “Historia de Yucatán”, Diego López
Cogolludo relató que los primeros Franciscanos encontraron numerosos indígenas
con las orejas “podridas”. En 1909,
Lindeberg y Paranhos de forma
independiente descubrieron la presencia del parasito del tipo L. tropica en las
lesiones de trabajadores del nordeste del Brasil. Un año después Splendore observó dichos
parásitos en las lesiones mucosas de los enfermos de la misma zona. Viena en 1911, al notar las diferencias
clínicas con el botón de oriente, creó la especie L. brasiliensis como el
agente etiológico de la leishmaniasis americana. En México, Seidelin en 1912 observa la
frecuencia de las lesiones en los
trabajadores del chicle en la zona de Yucatán y la denomina “úlcera de los
chicleros” que en 1953, Biagi, propuso a L. trópica mexicana como el agente
etiológico y en 1955 mediante estudios
serológicos, Garnham y Adler, la elevaron a categoría de especie denominándole Leishmania
mexicana.
 |
| Leishmania |
En su ciclo biológico
leishmania pasa por dos estadios: amastigote y promastigote. El primero esta desprovisto de flagelo y es
la forma parasitaria y sólo se observa en los tejidos de los vertebrados
infectados, o en cultivo de tejidos. Los
amastigotes en las leishmaniasis cutáneas se encuentran infestando células del
sistema reticuloendotelial de la piel de los mamíferos y los del kala-azar se
encuentran parasitando el sistema reticuloendotelial de bazo, hígado, médula ósea. En cambio en la leishmaniasis tegumentaria el
transmisor ingiere de la lesión del hospedero los amastigotes que pasan al tubo
digestivo del insecto y evolucionan a premastigotes, se multiplican por fisión
binaria forma de reproducción asexual de las células procariotas) y se acumulan
en la proboscis (en los invertebrados, el término generalmente se refiere a
piezas bucales tubulares utilizados para la alimentación y la succión) del
transmisor. El estado promastigote posee
un flagelo y tiene forma de huso. El
ciclo biológico se completa cuando el Phlebotomus (Lutzomyia) infectado pica a
un hospedero susceptible, transmitiéndole los promastigotes que al ser
fagocitados por el macrófago, pierden su flagelo, se redondean y empiezan a
dividirse por fisión binaria hasta llenar el citoplasma de la célula,
haciéndola estallar e invadiendo nuevas células.
Para que la enfermedad
se manifieste se necesitan factores inherentes tanto del hospedero como del
parasito. Para que Leishmania sea
infectante se necesita la capacidad para inhibir las enzimas lisosomales de las
células fagocíticas así como su dosis de inóculo. Se atribuye a una toxina que afecta a los
nervios periféricos la ausencia de dolor de las lesiones. La cronicidad
y diseminación de las lesiones van a depender de las condiciones de inmunidad del
hospedero.
La Leishmaniasis es una
enfermedad de distribución mundial, que afecta a 88 países: 72 de ellos son
países en vías de desarrollo, y 13 están entre los países más pobres del mundo.
El 90% de la leishmaniasis visceral se
diagnostica en 5 países: Bangladesh, India, Nepal, Sudan y Brasil; el 90%
de la leishmaniasis cutánea se diagnostica en 7 países: Afganistán, Argelia,
Brasil, Irán, Perú, Arabia Saudí y Siria.
La OMS estima que 350 millones de personas están en riesgo de leishmaniasis. Anualmente la incidencia se estima de alrededor de 1 a 1.5 millón de casos de leishmaniasis cutánea y 500 000 casos de leishmaniasis visceral. La prevalencia es de aproximadamente 12 millones de personas infectadas. Por lo regular es más frecuente en las zonas rurales que en las urbanas.
La OMS estima que 350 millones de personas están en riesgo de leishmaniasis. Anualmente la incidencia se estima de alrededor de 1 a 1.5 millón de casos de leishmaniasis cutánea y 500 000 casos de leishmaniasis visceral. La prevalencia es de aproximadamente 12 millones de personas infectadas. Por lo regular es más frecuente en las zonas rurales que en las urbanas.
Los reservorios van a
depender de la localidad, se incluye a
los seres humanos (en la leishmaniasis visceral en la india es el único
reservorio), roedores salvajes, algunos ciervos acuáticos, perezosos, zarigüeya
y carnívoros; incluyendo al perro doméstico.
Su periodo de
incubación va de unas semanas a varios meses en la leishmaniasis cutánea y mucocutanea;
en la leishmaniasis visceral por lo regular es de dos a seis meses con límites
de diez días a varios años.
No es típica la
transmisión de una persona a otra, en la leishmaniasis; pero en muchos
pacientes la curación es espontanea para la variedad cutánea.
La susceptibilidad probablemente
es general, para ambas variedades, desconociéndose los factores que causan la
enfermedad tardía mutilante, como la espundia.
En la variedad cutánea
y mucocutanea la enfermedad comienza con una elevación eruptiva que se agranda
y típicamente se transforma en úlcera indolora.
La lesión pueden ser únicas o múltiples y, ocasionalmente, no ulceradas
y difusas. Pueden cicatrizar
espontáneamente en el término de semanas o meses o persistir un año o más. En algunas personas, diversas especies parásitas,
se diseminan y producen lesiones de la mucosa (espundia), incluso años después
que ha curado la lesión cutánea primaria.
Estas secuelas, que afectan a los tejidos nasofaríngeos, se caracterizan
por destrucción progresiva de los tejidos y a menudo por la presencia de pocos parásitos;
pueden ser muy desfigurantes.
 |
| Diferentes presentaciones clínicas de la leishmaniasis |
En la variedad visceral
se caracteriza por fiebre, crecimiento de hígado y bazo, afección de los
ganglios linfáticos, anemia, disminución de los glóbulos blancos y plaquetas,
adelgazamiento y debilidad progresiva.
El cuadro clínico manifiesto, si no es tratado, por lo común termina en
la muerte. La fiebre tiene comienzo
gradual o repentino, es persistente e irregular, a menudo con dos
exacerbaciones al día; después se alterna con ausencia de fiebre y fiebre
baja. Las lesiones dérmicas después de
la variedad visceral pueden surgir después de la curación aparente de la
enfermedad sistémica.
El diagnostico se
realiza por la identificación microscópica del amastigote del material obtenido
de las lesiones y por cultivo del
promastigote en medios adecuados. La
prueba intradérmica (reacción de Montenegro) pierde su utilidad en caso de
lesiones muy tempranas o en la enfermedad inactiva. La prueba de ELISA es útil en el diagnóstico
de la leishmaniasis mucocutanea. En la
variedad visceral el diagnóstico se hace preferentemente por cultivo del
microrganismo en material de Biopsia o aspirado o por demostración de los
amastigotes intracelulares (cuerpos de Leisman-Donovan) en frotis teñidos de
material de médula ósea, bazo, hígado, ganglios linfáticos o sangre.
Las medidas preventivas
pueden ser aplicadas, de forma eficiente, cuando se conocen los hábitos de los
insectos, que incluyen: Detección sistémica de los casos y tratamiento rápido,
aplicación periódica de insecticidas de acción residual, eliminación de
basureros y otros sitios que sirvan de criaderos de flebótomos del Viejo Mundo,
en el nuevo mundo evitar entrar a zonas muy boscosas e infestadas de
flebótomos, especialmente después del atardecer; utilice repelentes de insectos
y ropa protectora si la exposición a los flebótomos es inevitable, aplicar
medidas ambientales y de habitad selváticas (si es posible, la desforestación).
En caso de un paciente
positivo es importante notificar a las autoridades de salud, identificar el
ciclo de transmisión local e irrumpirlo de la manera más práctica posible,
brindar el tratamiento específico, en especial y de forma rápida en las zonas
en donde es común la enfermedad de las mucosas.
En la forma visceral se debe tener precaución con la sangre y los
líquidos corporales.
No hay comentarios:
Publicar un comentario